Artmış Bağırsak Geçirgenliği ve Zonulin
Yazı Boyutunu Değiştirebilirsiniz
 Son yıllarda yapılan çalışmalar; bağırsakların, besinleri sindirim ve emilimi ile su ve elektrolit homeostazisi yanı sıra mukozal bariyer aracılığı ile vücuda yabancı çevresel antijenlerin girişinin önlenmesinde de anahtar rol oynadığını göstermiştir (1). Bağırsak geçirgenliğinin artması sonucu bir çok hastalık gelişebilir ve bu hastalıklar yalnız bağırsak hastalıkları olmayabilir. Tip I Diabetes Mellitus, Multiple Skleroz, Allerji gibi otoimmun hastalıkların yanı sıra birçok hastalık da artmış bağırsak geçirgenliğinin sonucu ortaya çıkabilir. Birçok hastalığın bağırsaklardan başladığını kanıtlayan birçok bulgu vardır. Ancak bu hastalıkların bağırsaklarda lokalize olmaması dikkat çekicidir ve diğer organlarda da oluşabilir.
Son yıllarda yapılan çalışmalar; bağırsakların, besinleri sindirim ve emilimi ile su ve elektrolit homeostazisi yanı sıra mukozal bariyer aracılığı ile vücuda yabancı çevresel antijenlerin girişinin önlenmesinde de anahtar rol oynadığını göstermiştir (1). Bağırsak geçirgenliğinin artması sonucu bir çok hastalık gelişebilir ve bu hastalıklar yalnız bağırsak hastalıkları olmayabilir. Tip I Diabetes Mellitus, Multiple Skleroz, Allerji gibi otoimmun hastalıkların yanı sıra birçok hastalık da artmış bağırsak geçirgenliğinin sonucu ortaya çıkabilir. Birçok hastalığın bağırsaklardan başladığını kanıtlayan birçok bulgu vardır. Ancak bu hastalıkların bağırsaklarda lokalize olmaması dikkat çekicidir ve diğer organlarda da oluşabilir.
Zonulin bağırsak geçirgenliği artışını gösteren önemli bir biyobelirteçtir.
Bağırsak duvarı, bağırsağın içini çevreleyen tek hücreli kalın epitelyal hücrelerden oluşmuştur ve insan vücudu ile dış dünya arasındaki en geniş yüzeyli bariyerdir. Bu bariyerin bütünlüğünün korunması ve geçirgenliğin kontrolü immün sistemin regülasyonu ve patojenlere karşı korunmada çok önemlidir.
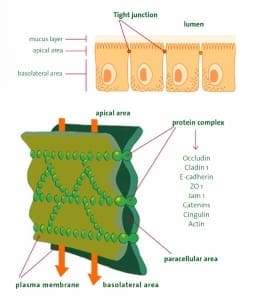 Bağırsak lümeninden dolaşıma geçişte iki yol bulunur. İlki enterositlerin fırçamsı kenarları boyunca ‘’transporter’’ (taşıyıcılar) aracılığı ile olur, buna transsellüler yol denir, pek çok besin maddesinin emilimi bu yolla olur. İkinci yol; hücreler arası boşluklardan parasellüler geçiştir. Bu yoldan iyonlar, suda çözünen moleküller ve nadir mikroorganizmalar geçiş yapar (2,3). Parasellüler geçiş ‘’tight junctions’’ (sıkı kavşaklar) adı verilen protein yapıda kapılar tarafından kontrol edilir. Bu dinamik yapılar beslenme durumu, fiziksel aktivite, hormonal ve sinirsel sinyaller ve inflamatuvar medyatörler ile uyumlu şekilde açılır ve kapatılır (4,5). Bağırsak sıkı kavşakları (tight junctions); besinlerin optimal emilimi ve transportu yanı sıra vücuda yabancı antijenlere karşı tolerans ve immunite arasında denge oluşumunun sağlanmasında da görev alır. Günümüzde bağırsak sıkı bağlantılarının yapısı hakkında önemli bilgiler varolmakla birlikte, fizyolojisi ve patofizyolojisi hakkında bilgilerimiz nispeten sınırlıdır. Zonulin; bu sıkı kavşaklarda anahtar pozisyonunda fizyolojik ve reverzibl bir modülatördür. Bu protein mukozada oluşur ve bağırsak geçirgenliğini direkt olarak kontrol eder (2,6,7). Bağırsak lümenindeki bakteriler veya gıdalardaki tetikleyici maddeler (ör: gluten) gibi uyaranlara yanıt olarak Zonulin lümene salınır ve epitel hücrelerinin apikal yüzeylerindeki reseptörlere bağlanarak sıkı kavşakların bütünlüğünün bozulmasına neden olan yolakları başlatır (8,9). Hücre içi sıkı bağlantılarının bilinen tek fizyolojik modülatörü Zonulin’in keşfi, bağırsak epitelyal parasellüler yolağın, karmaşık mekanizmalarını ve genetik olarak yatkın kişilerde bu mekanizmalardaki bozuklukların, otoimmün hastalıklara neden olduğunu anlamamızı sağladı.
Bağırsak lümeninden dolaşıma geçişte iki yol bulunur. İlki enterositlerin fırçamsı kenarları boyunca ‘’transporter’’ (taşıyıcılar) aracılığı ile olur, buna transsellüler yol denir, pek çok besin maddesinin emilimi bu yolla olur. İkinci yol; hücreler arası boşluklardan parasellüler geçiştir. Bu yoldan iyonlar, suda çözünen moleküller ve nadir mikroorganizmalar geçiş yapar (2,3). Parasellüler geçiş ‘’tight junctions’’ (sıkı kavşaklar) adı verilen protein yapıda kapılar tarafından kontrol edilir. Bu dinamik yapılar beslenme durumu, fiziksel aktivite, hormonal ve sinirsel sinyaller ve inflamatuvar medyatörler ile uyumlu şekilde açılır ve kapatılır (4,5). Bağırsak sıkı kavşakları (tight junctions); besinlerin optimal emilimi ve transportu yanı sıra vücuda yabancı antijenlere karşı tolerans ve immunite arasında denge oluşumunun sağlanmasında da görev alır. Günümüzde bağırsak sıkı bağlantılarının yapısı hakkında önemli bilgiler varolmakla birlikte, fizyolojisi ve patofizyolojisi hakkında bilgilerimiz nispeten sınırlıdır. Zonulin; bu sıkı kavşaklarda anahtar pozisyonunda fizyolojik ve reverzibl bir modülatördür. Bu protein mukozada oluşur ve bağırsak geçirgenliğini direkt olarak kontrol eder (2,6,7). Bağırsak lümenindeki bakteriler veya gıdalardaki tetikleyici maddeler (ör: gluten) gibi uyaranlara yanıt olarak Zonulin lümene salınır ve epitel hücrelerinin apikal yüzeylerindeki reseptörlere bağlanarak sıkı kavşakların bütünlüğünün bozulmasına neden olan yolakları başlatır (8,9). Hücre içi sıkı bağlantılarının bilinen tek fizyolojik modülatörü Zonulin’in keşfi, bağırsak epitelyal parasellüler yolağın, karmaşık mekanizmalarını ve genetik olarak yatkın kişilerde bu mekanizmalardaki bozuklukların, otoimmün hastalıklara neden olduğunu anlamamızı sağladı.
Bağırsak lümeninden dolaşıma geçişte iki yol bulunur. İlki enterositlerin fırçamsı kenarları boyunca ‘’transporter’’ (taşıyıcılar) aracılığı ile olur, buna transsellüler yol denir, pek çok besin maddesinin emilimi bu yolla olur. İkinci yol; hücreler arası boşluklardan parasellüler geçiştir. Bu yoldan iyonlar, suda çözünen moleküller ve nadir mikroorganizmalar geçiş yapar (2,3). Parasellüler geçiş ‘’tight junctions’’ (sıkı kavşaklar) adı verilen protein yapıda kapılar tarafından kontrol edilir. Bu dinamik yapılar beslenme durumu, fiziksel aktivite, hormonal ve sinirsel sinyaller ve inflamatuvar medyatörler ile uyumlu şekilde açılır ve kapatılır (4,5). Bağırsak sıkı kavşakları (tight junctions); besinlerin optimal emilimi ve transportu yanı sıra vücuda yabancı antijenlere karşı tolerans ve immunite arasında denge oluşumunun sağlanmasında da görev alır. Günümüzde bağırsak sıkı bağlantılarının yapısı hakkında önemli bilgiler varolmakla birlikte, fizyolojisi ve patofizyolojisi hakkında bilgilerimiz nispeten sınırlıdır. Zonulin; bu sıkı kavşaklarda anahtar pozisyonunda fizyolojik ve reverzibl bir modülatördür. Bu protein mukozada oluşur ve bağırsak geçirgenliğini direkt olarak kontrol eder (2,6,7). Bağırsak lümenindeki bakteriler veya gıdalardaki tetikleyici maddeler (ör: gluten) gibi uyaranlara yanıt olarak Zonulin lümene salınır ve epitel hücrelerinin apikal yüzeylerindeki reseptörlere bağlanarak sıkı kavşakların bütünlüğünün bozulmasına neden olan yolakları başlatır (8,9). Hücre içi sıkı bağlantılarının bilinen tek fizyolojik modülatörü Zonulin’in keşfi, bağırsak epitelyal parasellüler yolağın, karmaşık mekanizmalarını ve genetik olarak yatkın kişilerde bu mekanizmalardaki bozuklukların, otoimmün hastalıklara neden olduğunu anlamamızı sağladı.
İyi işleyen bağırsak absorbsiyonu beslenmede yaşamsal öneme sahiptir. Diğer yandan bağırsak mukozası, vücudu patojen bakterilerden ve çevresel kirliliklerden korur. Bu nedenle bağırsaktan kontrollü geçirgenlik sağlık için büyük öneme sahiptir. Çevresel tetikleyicilerin uzun süreli Zonulin upregülasyonu, bağırsak geçirgenliğinin artmasına, bağırsaktaki antijenlerin submokozaya sürekli geçişine neden olur. Eğer bağırsak geçirgenliği artarsa çok miktarda zararlı madde dolaşım sistemine geçer. Öncelikle bağırsak mukozası enfekte olur. Bu durum uzun dönemde bağırsak mukozasının hasarına yol açar. Böylelikle bağırsakların geçirgenliği daha da artar ve kısır döngüye girilir, bu geçirgenlik artışı immun sistemin yoğun reaksiyonuna neden olur. Bağırsak geçirgenliğinin artması sonucu zararsız gıda maddeleri dolaşıma geçerek, gıda alerjilerine veya gıda intoleransına yol açar ve yakınmalar başlar. Ek olarak diğer immünolojik reaksiyonlarda gelişir. Aşırı geçirgen ya da sızdıran bağırsak adı verilen bu durum uzun dönemde vücudun kendi hücre yapı ve organları ile ilişkili otoantikorlar üretir ve otoimmun hastalıklara neden olur. Özellikle Tip I Diyabetes Mellitus, Multiple Skleroz, Romatoid Artrit, Çölyak Hastalığı ve daha birçok otoimmun hastalık, artmış bağırsak geçirgenliği nedeni ile gelişebilir (1,10). Bağırsaktan aşırı geçirgenlik ayrıca etyolojisi iyi bilinmeyen irritabl bağırsak sendromu gibi kronik hastalıklarla da ilişkilendirilmiştir. Bakterilerin dolaşıma geçmesi, karaciğerde inflamasyon yoluyla, yağlı karaciğer hastalığı, Tip II Diyabetes Mellitus ve kardiyovasküler hastalıklar gibi bir çok metabolik durumda da nedensel rol oynamaktadır. Bağırsak bariyerinin bozulması, bakteriyel toksinler ve sitokin kaskadları aracılığı ile nöroinflamasyon ve depresyon gelişimi ile de ilişkilendirilmiştir (11).
Zonulin İle İlişkili Olan Bazı Hastalıklar (3)
| Otoimmün Hastalıklar:
Çölyak Hastalığı Ankilozan Spondilit Romatoid Artrit Crohn Hastalığı SLE |
Kanserler: Akciğer Kanseri Meme Kanseri Pankreas Kanseri Over Kanseri Beyin Kanseri |
Sinir Sistemi Hastalıkları: Kronik İnflamatuar Demiyelinizan Nöropati Multiple Skleroz Şizofreni
|

Çölyak hastalığında bağırsak permeabilitesi artmıştır ve Zonulin’in upregülasyonu sonucudur. Dermatitis Herpetiformis hastalarında, minimal bağırsak hasarı varken, Zonulin’in yüksek düzeyleri, Zonulin ilişkili anormal bağırsak geçirgenliğinin, glutene bağlı hastalıkların patogenezinde erken rol oynadığını desteklemektedir (12). Gluten kaynaklı gliadinin, nonçölyak hastalarda dahi, Zonulin salınımını stimüle ettiği ve bağırsak geçirgenliğini arttırdığı gösterilmiştir (9). Tip I diyabetli hastaların önemli bir bölümünde (bir çalışmada %42) yüksek Zonulin seviyeleri, hastalık başlangıcından birkaç yıl önce gösterilmiştir (12). Bu durum otoimmün diyabette bağırsak aşırı geçirgenliğinin nedensel bir rolü ve hastalığın başlangıcı ve ilerlemesinde Zonulin’in prediktif değeri ile uyumludur (11,13). Klinik öncesi çalışmalar, Tip I Diyabetes Mellitus patogenezinde Zonulin aracılı hiperpermeabilitenin rolünü desteklemektedir. Bozulmuş bağırsak bariyer fonksiyonu ve yüksek Zonulin düzeylerinin, vücut kitle indeksinden bağımsız olarak insülin direnci ve Tip II Diyabetes Mellitus ile ilişkili olduğu saptanmıştır (14,15). Zonulin düzeyinin astım hastalarının yaklaşık % 40’ında yüksek bulunmuştur ve bu hastalarda bağırsak geçirgenliği artmıştır. Normalde sıkı kavşaklarda önlenecek spesifik antijenlerin ve irritanların parasellüler geçiş yoluyla dolaşıma geçmesi ve allerjik reaksiyonların başlaması astıma yol açmaktadır (16)
Çalışmalarda bağırsak geçirgenliğinin altın standartı olan laktuloz-mannitol testi ile Zonulin düzeylerinin kuvvetli korelasyonu gösterilmiştir. Zonulin bozulmuş bağırsak geçirgenliğinin gösterilmesinde çok iyi bir biyobelirteçtir. Seruma beyin ve akciğer gibi organlardan da Zonulin salınması nedeniyle dışkı örneği daha uygundur. Hastalar örnek vermeden bir ay öncesine kadar antibiyotik ve iki hafta öncesine kadar da probiyotik almamış olmalıdır.
REFERANSLAR:
1- Fasano A..Ann N.Y. Zonulin, regulation of tight junctions, and autoimmune diseases. Acad Sci.2012 Jul:1258(1):25-33
2- Fasano A. Physiological, Pathological, and Therapeutic Implications of Zonulin-Mediated Intestinal Barrier Modulation. Am J Pathology 2008;173:1243–1252.
3- Fasano A. Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Physiol Rev 2011;91:151–175
4- Arrieta MC, et al. Alterations in intestinal permeability. Gut 2006;55:1512–1520.
5- Lamprecht M, Frauwallner A. Exercise, intestinal barrier dysfunction and probiotic supplementation. Med Sport Sci 2012;59:47–56.
6- Wang W, et al. Human zonulin, a potential modulator of intestinal tight junctions. J Cell Sci 2000;113:4435–4440.
7- Fasano A. Intestinal Permeability and its Regulation by Zonulin: Diagnostic and Therapeutic Implications. Clin Gastroenterol Hepatol 2012;10:1096–1100.
8- El Asmar R, et al. Host-dependent zonulin secretion causes the impairment of the small intestine barrier function after bacterial exposure. Gastroenterol 2002;123:1607–1615.
9- Tripathi A, et al. Identification of human zonulin, a physiological modulator of tight junctions, as prehaptoglobin-2. Proc Natl Acad Sci 2009;106:16799-16804.
10- Fasano A, Shea-Donohue T. Mechanisms of disease: the role of intestinal barrier function in the pathogenesis of gastrointestinal autoimmune diseases. Nat Clin Pract Gastroenterol Hepatol 2005;2:416–422.
11- Leonard B, Maes M. Mechanistic explanations how cell-mediated immune activation, inflammation and oxidative and nitrosative. Neurosci Biobehav Rev 2012;36(2):764–785
12- Smecuol E, et al. Permeability, zonulin production, and enteropathy in dermatitis herpetiformis. Clin Gastroenterol and Hepatol 2005;3:335–341.
13- De Kort S, et al. Leaky gut and diabetes mellitus: what is the link? Obes Rev 2011;12:449–458.
14- Moreno-Navarrete JM, et al. Circulating Zonulin, a Marker of Intestinal Permeability. PLOS One 2012;7:e37160.
15- Zhang D, et al. Circulating zonulin levels in newly diagnosed Chinese type 2 diabetes patients. Diabetes Res Clin Pract 2014;106:312–318.
16- Hijazi Z, Molla AM, Al-Habashi H, Muawad WM, Molla AM, Sharma PN. Intestinal permeability is increased in bronchial asthma. Arch Dis Child 89: 227–229, 2004.


